Vývoj softwaru pro zdravotnické prostředky (SaMD/MDSW)
Komplexní vývoj softwaru pro zdravotnické prostředky
| Od konceptu po certifikaci
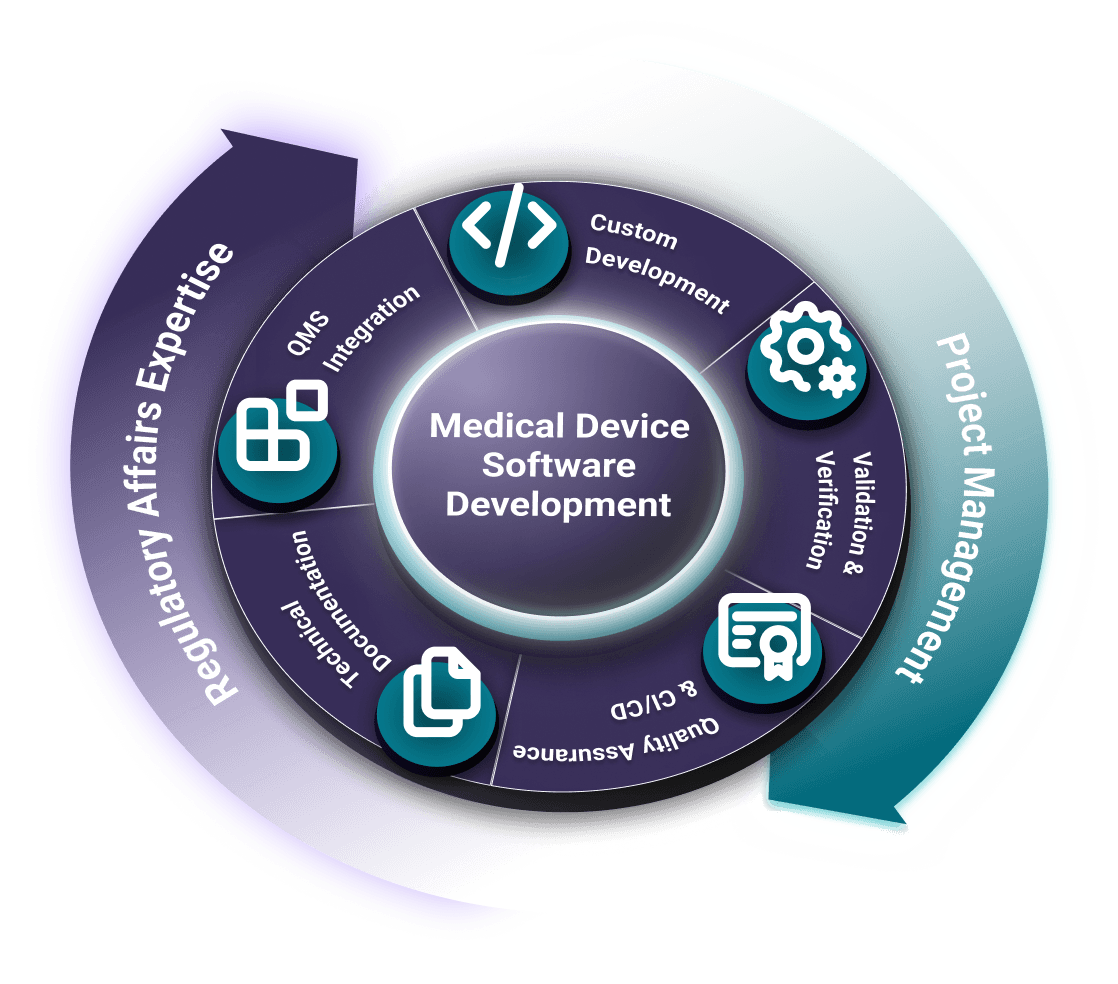
QMLogic je vaším důvěryhodným partnerem pro vývoj softwaru pro zdravotnické prostředky (MDSW/SaMD). Poskytujeme kompletní technickou, regulační a projektovou podporu a zajišťujeme, aby váš software pro zdravotnické prostředky byl bezpečný, účinný a v souladu s mezinárodními normami a předpisy, jako jsou IEC 62304, ISO 13485, ISO 14971, FDA 21 CFR a EU MDR.
Od koncepce a návrhu, ověření a validace po předložení regulačním orgánům a dohled po uvedení na trh provázíme společnosti zabývající se zdravotnickými prostředky celým životním cyklem vývoje softwaru. Naše řešení jsou vždy připravena k auditu, vyhovují předpisům a jsou hladce integrována do vašeho systému řízení kvality (QMS).

Služby vývoje softwaru pro zdravotnické prostředky
Jsme vývojáři tělem i duší. Náš tým denně vytváří sofistikovaný software pomocí nejmodernějších technologií, jako jsou React.js, Next.js, Spring Boot a .NET. Vývoj není něco, co outsourcujeme; je to naše klíčová odbornost, která je hladce integrována s našimi znalostmi v oblasti regulace, abychom od prvního dne vytvářeli inovativní řešení v souladu s předpisy.
- Soulad zabudovaný do každého řádku kódu
- Vývojáři a odborníci na předpisy v jednom týmu
- Soulad s normou IEC 62304 již od návrhu
- Integrace s normou ISO 14971 pro řízení rizik
- Návrh s ohledem na kybernetickou bezpečnost podle normy IEC 81001-5-1
- Znalost React, Spring Boot, .NET
- Moderní stack, bezpečnost na lékařské úrovni
Software nevytváříme izolovaně – slaďujeme jej s vaším systémem řízení kvality a zajišťujeme, aby každý řádek kódu podporoval dodržování předpisů, efektivitu a kontinuitu podnikání.
Odbornost v oblasti regulace při vývoji softwaru pro zdravotnické prostředky
Naše odborné znalosti v oblasti regulace zajišťují, že váš software je připraven na audit, validován a v souladu s klíčovými normami, včetně:

IEC 62304
Soulad s životním cyklem softwaru
Definuje požadované procesy vývoje a údržby pro SaMD/MDSW, zajišťuje bezpečnost, sledovatelnost a regulační schválení.

ISO 13485
QMS pro lékařský software
Poskytuje rámec pro řízení kvality, který zajišťuje soulad vývoje softwaru s globálními normami pro zdravotnické prostředky.

ISO 14971
Integrace řízení rizik
Zajišťuje, že identifikace, hodnocení a kontrola rizik jsou začleněny do životního cyklu softwaru, čímž chrání pacienty a uživatele.

ISO 80002-2
Validace počítačových systémů
Poskytuje pokyny pro validaci počítačových systémů a softwaru a zajišťuje spolehlivý výkon a regulační přijatelnost.

EU-MDR
Evropské nařízení o zdravotnických prostředcích
Stanoví požadavky na označení CE pro software zdravotnických prostředků, které se týkají bezpečnosti, výkonu a dozoru po uvedení na trh.

21 CFR Part 820
Soulad s předpisy USA
Část 11 upravuje elektronické záznamy a podpisy, zatímco část 820 zajišťuje soulad systému kvality pro software regulovaný FDA.

FDA 510(k)
Povolení pro přístup na trh
Prokazuje podstatnou rovnocennost softwaru pro zdravotnické prostředky, což umožňuje vstup na trh USA.

ISO/IEC 27001
Bezpečnost informací
Poskytuje celosvětově uznávaný rámec pro správu bezpečnosti informací a zajišťuje, že software pro zdravotnické prostředky chrání citlivé zdravotní údaje.

IEC 81001-5-1
Kybernetická bezpečnost zdravotnického softwaru
Zabývá se konkrétně kybernetickou bezpečností zdravotnického softwaru se zaměřením na bezpečné navrhování, vývoj a údržbu softwaru pro zdravotnické prostředky.
Díky kombinaci technické odbornosti a dokonalé znalosti předpisů pomáháme společnostem v oblasti zdravotnických technologií:
Navrhovat, vytvářet a validovat SaMD s integrovanou shodu s předpisy
Vytvářet technickou dokumentaci připravenou k auditu od samého začátku
Urychlit certifikaci EU MDR a schválení FDA
Uvedení na trh rychleji díky škálovatelnému, kompatibilnímu a budoucnosti odolnému softwarovému řešení
Náš jedinečný přístup zajišťuje, že každý řádek kódu podporuje nejen vaše obchodní cíle, ale také regulační rámec, který řídí váš úspěch na trhu. Od koncepce po certifikaci vám pomáháme navrhovat, vytvářet, ověřovat a dokumentovat váš SaMD pro rychlejší a hladší uvedení na trh.
Proč QMLogic pro vývoj softwaru pro zdravotnické přístroje?

Prokázané úspěchy
Realizovali jsme řadu úspěšných a plně kompatibilních projektů vývoje SaMD, od počátečního konceptu až po dohled po uvedení na trh, a to jak pro start-upy, tak pro zavedené společnosti v oblasti zdravotnických technologií.
Integrace projektového řízení od začátku do konce
Naše specializované služby projektového řízení zajišťují efektivní koordinaci, transparentní komunikaci, sledování milníků a proaktivní řízení rizik v průběhu celého vývojového cyklu.
Odborné znalosti v oblasti regulace na globálních trzích
Rozsáhlé znalosti norem IEC 62304, ISO 13485, ISO 14971, EU MDR a FDA 21 CFR 820 zajišťují, že váš software splňuje všechny nezbytné regulační a compliance požadavky po celém světě.
Kybernetická bezpečnost a řízení rizik
Každá fáze vývoje je úzce sladěna s normami ISO 14971 pro řízení rizik a IEC 81001-5-1 pro kybernetickou bezpečnost, což zajišťuje bezpečnost pacientů a ochranu dat od samého začátku.
Přizpůsobitelná a škálovatelná řešení
Ať už spouštíte MVP, rozšiřujete se na komplexní platformu nebo vstupujete na nové globální trhy, náš přístup k vývoji a dodržování předpisů se může flexibilně přizpůsobit vašim měnícím se obchodním a technickým potřebám.
Integrace a digitalizace QMS
Vaše procesy vývoje softwaru budou hladce sladěny s vaším systémem řízení kvality (QMS) v souladu s normou ISO 13485. Nabízíme také podporu při implementaci softwaru QMS a digitalizaci za účelem modernizace vašich operací.
Jste připraveni vyvinout software pro vaše zdravotnické zařízení?
Ať už jste startup spouštějící své první SaMD nebo zavedený výrobce rozšiřující své portfolio, pomůžeme vám urychlit vývoj a zároveň zajistit dodržování předpisů.
Reference | Odbornost v oblasti softwaru pro zdravotnické prostředky
S Václavem jsem spolupracoval na činnostech řízení rizik projektů vývoje zdravotnických prostředků. Jeho schopnost rychle pochopit výzvy a dokončit úkol/projekt je pozoruhodná. Kromě toho je chvályhodná jeho schopnost navrhovat a vyvíjet softwarová řešení pro zlepšení efektivity projektů. Považuji Václava za flexibilního, spolehlivého a na kvalitu orientovaného. Proto jsem si práci s Václavem opravdu užil a těším se na další spolupráci s ním.
Měl jsem to potěšení pracovat s Václavem během našeho vývoje zdravotnického produktu pro společnost Merck. Zjistil jsem, že Václav je velmi profesionální a oddaný. Jeho smysl pro detail a jeho technické/lékařské znalosti přinesly projektu nesmírně cenné vstupy. Spolupráce s Václavem byla opravdu potěšením a vřele ho doporučuji.
Váš důvěryhodný partner ve všech fázích životního cyklu softwaru pro zdravotnické prostředky
Získejte konzultaci zdarma
Zeptejte se na vše, co potřebujete vědět o lékařském softwaru, certifikaci CE nebo MDR.

